Chirurgia
Chirurgia robotica
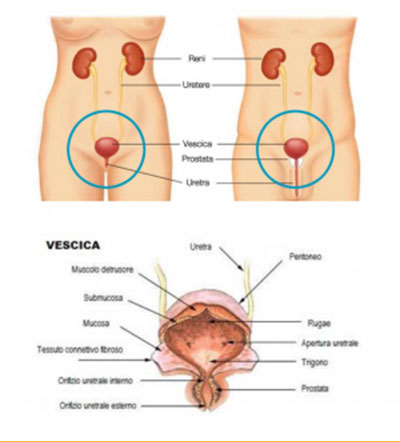 La vescica urinaria è un organo muscolare cavo posto nel bacino, deputato alla raccolta dell’urina prodotta dai reni che vi giunge attraverso gli ureteri. Dalla vescica l’urina viene periodicamente espulsa all’esterno attraverso l’uretra.
La vescica urinaria è un organo muscolare cavo posto nel bacino, deputato alla raccolta dell’urina prodotta dai reni che vi giunge attraverso gli ureteri. Dalla vescica l’urina viene periodicamente espulsa all’esterno attraverso l’uretra.
Il muscolo che forma le pareti della vescica è detto muscolo detrusore, un muscolo liscio la cui attività è regolata da fibre nervose che percepiscono il riempimento vescicale e lo comunicano al sistema nervoso centrale.L’uretra decorre attraverso un diaframma urogenitale costituito da muscolatura striata sottoposta a controllo volontario, o sfintere esterno. Il processo di emissione dell’urina, detto minzione, porta allo svuotamento periodico della vescica urinaria per mezzo di un riflesso automatico del midollo spinale, sempre mediato dal sistema nervoso centrale
l tumore della vescica
Il tumore della vescica, in costante aumento nei Paesi industrializzati, rappresenta circa il 70% delle forme tumorali a carico dell’apparato urinario e circa il 3% di tutti i tumori. È più comune tra i 60 e i 70 anni, ed è tre volte più frequente negli uomini che nelle donne. La sopravvivenza a cinque anni supera, in Italia, il 70% dei casi.
Per il tumore della vescica sono stati individuati i seguenti fattori di rischio: il fumo di sigaretta, l’esposizione cronica alle amine aromatiche e nitrosamine (frequente nei lavoratori dell’industria tessile, dei coloranti, della gomma e del cuoio), l’assunzione di farmaci come la ciclofosfamide e l’infezione da parassiti come Bilharzia e Schistosoma haematobium, diffusi in alcuni paesi del Medio Oriente (Egitto in particolare). Anche la dieta gioca un ruolo importante: fritture e grassi consumati in grande quantità sono infatti associati a un aumentato rischio di ammalarsi di tumore della vescica. Esistono infine prove a favore di una componente genetica quale fattore di rischio predisponente. Il tipo più frequente di tumore della vescica è il cosiddetto carcinoma a cellule uroteliali che costituisce circa il 97% dei casi. Altri tipi di cancro alla vescica sono rappresentati dall’adenocarcinoma e dal carcinoma squamoso primitivo, ma sono decisamente meno frequenti. Quest’ultimo è spesso associato alle infezioni da parassiti.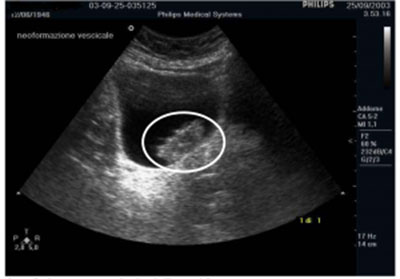
Il tumore della vescica si forma più spesso sulle pareti laterali dell’organo (Fig 3): può avere una forma papillare (cioè come una vegetazione) nella maggior parte dei casi (75%) oppure una forma piatta o nodulare (carcinoma in situ, CIS).
I sintomi con cui si può presentare il tumore della vescica sono comuni anche ad altre malattie che colpiscono l’apparato urinario.
Manifestazioni frequenti sono la presenza di sangue nelle urine e la formazione di coaguli, la sensazione di bruciore alla vescica quando si comprime l’addome, la difficoltà e il dolore a urinare, la maggior facilità a contrarre infezioni. Con la progressione della malattia questi disturbi possono diventare importanti.
Non sempre il suo comportamento è prevedibile per quanto riguarda le ricadute locali e l’aggressività.
Non esistono al momento programmi di screening o metodi di diagnosi precoce scientificamente affidabili. Occorre quindi mettere in atto misure di prevenzione legate alle abitudini di vita che consistono nell’abolizione del fumo e in una dieta sana ed equilibrata.
Il tipo di anestesia per la cistectomia radicale robotica, come per tutti gli interventi di chirurgia maggiore, è l’anestesia generale.
La prevenzione dei fenomeni trombotici e tromboembolici viene attuata dal posizionamento, prima dell’inizio dell’intervento, di calze elastiche agli arti inferiori, dalla somministrazione di un farmaco anti coagulante sotto cute a partire dalla sera successiva all’intervento e prolungata per 20-30 giorni, nonché dalla precoce mobilizzazione del paziente stesso.
Si ha indicazione all’ intervento di cistectomia radicale in quadri di neoplasia vescicale ad alto rischio di progressione, in particolare quando:
- il tumore vescicale invade la parete muscolare
- il tumore occupa una superficie vescicale ampia con concomitante Carcinoma in Situ
- si hanno recidive frequenti, nonostante una terapia intravescicale con antiblastici o BCG e TURV.
Il primo tempo dell’intervento consiste nella creazione dello
pneumoperitoneo: la cavità addominale deve essere riempita di anidride carbonica per creare una camera di lavoro per gli strumenti chirurgici robotici.
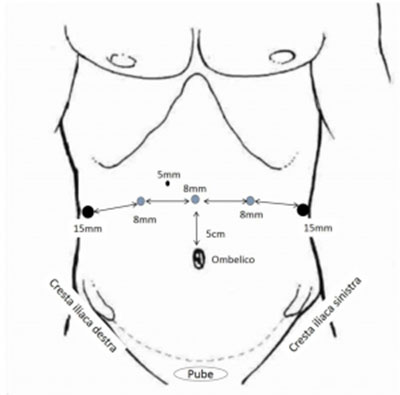 Una incisione di circa 2 cm a livello sopra-ombelicale consente di posizionare sotto visione diretta ed in maniera del tutto atraumatica il primo trocar robotico attraverso il quale si inserisce l’ottica che permetterà al chirurgo di eseguire l’intervento.
Una incisione di circa 2 cm a livello sopra-ombelicale consente di posizionare sotto visione diretta ed in maniera del tutto atraumatica il primo trocar robotico attraverso il quale si inserisce l’ottica che permetterà al chirurgo di eseguire l’intervento.
Si inseriscono successivamente in cavità peritoneale i successivi 6 trocar operativi, di cui tipicamente 4 gestiti dal primo operatore e 2 dall’assistente.
La premessa da considerare prima di descrivere l’intervento nei dettagli è che la tecnica robotica consente di operare con un ingrandimento visivo fino a circa 20 volte e con una visione a 3 dimensioni. Questo permette al chirurgo di apprezzare la profondità di campo, cosa non possibile ad esempio con la tecnica laparoscopica classica. La visione intraoperatoria robotica permette di riconoscere anche i più piccoli dettagli anatomici e di eseguire l’intervento con una accuratezza significativamente superiore a quanto sia possibile ottenere con la chirurgia classica a cielo aperto o con la chirurgia laparoscopica classica.
Il primo tempo operatorio è rappresentato dall’isolamento delle vescicole seminali, attraverso una piccola breccia eseguita nel peritoneo parietale che riveste il cavo del Douglas, al di sopra dell’intestino retto.
Completato l’isolamento delle vescicole seminali, dalla cavità peritoneale si accede allo spazio pelvico dove sono localizzate la vescica e la prostata (nell’uomo) e l’utero, le ovaie e la porzione anteriore della vagina nella donna.
Si procede quindi alla rimozione dei linfonodi pelvici (linfoadenectomia), a cui afferisce la linfa prodotta dalla vescica, bilateralmente. I linfonodi sono piccoli organelli che hanno la la funzione di filtrare liquidi e proteine provenienti da tutto l’organismo. Quando un organo si ammala di tumore è possibile che alcune cellule tumorali escano dai confini dello stesso e vengano catturate dai linfonodi più vicini. Per questo motivo in tutti i pazienti affetti da neoplasia vescicale candidati a cistectomia radicale la rimozione dei linfonodi viene eseguita al fine di ottenere una più precisa stadiazione della malattia ed anche perchè la rimozione di eventuali linfonodi ammalati può avere un valore terapeutico. La tecnica robotica permette di eseguire linfoadenectomie estremamente estese ed accurate e quindi la tecnica si presta ad essere utilizzata con successo anche in pazienti con tumore della vescica.
Completata la linfoadenectomia, si procede all’isolamento degli ureteri e alla loro disconnessione dalla vescica. I margini di resezione degli ureteri vengono immediatamente inviati al Servizio di Anatomia Patologica per assicurare l’assenza di malattia neoplastica a livello del tratto terminale degli ureteri. Successivamente si procede alla rimozione della vescica e della prostata (nell’uomo) oppure dell’utero, delle ovaie e della parete anteriore della vagina (nella donna) con una tecnica anterograda. Se viene rimossa la prostata, il paziente non sarà più in grado di eiaculare e quindi avere figli. Inoltre potrà avere problemi durante i rapporti sessuali. Anche le pazienti, in caso di rimozione dell’utero, non potranno più avere figli per via naturale. Inoltre, se il chirurgo rimuove parte della vagina, la qualità dei rapporti potrà risentirne. A seconda delle caratteristiche della malattia e dell’età del paziente si procede nell’isolamento e nella sezione dei peduconcoli vascolari vescicali e prostatici o vaginali ponendo la massima attenzione per salvaguardare i nervi deputati alla funzione sessuale, quando ciò risulta oncologicamente sicuro e indicato.
Si procede quindi alla sezione del plesso venoso di Santorini ed alla sua successiva sutura emostatica con punti posti sotto visione diretta. Si procede poi a sezionare l’uretra a livello dell’apice prostatico e a questo punto il pezzo operatorio, completamente liberato, viene riposto in un apposito contenitore (Endobag).
L’asportazione della vescica comporta di necessità l’esigenza di derivare le urine, non essendo più possibile la loro raccolta all’interno della vescica e la loro conseguente eliminazione. Ciascuna delle derivazioni urinarie indicate presenta peculiari benefici, svantaggi e possibili complicanze. L’intervento ha un durata di 3-6 ore a seconda della tecnica chirurgica adottata e delle condizioni anatomiche del paziente.
Il Suo Urologo Le consiglierà la derivazione urinaria più adatta alle Sue condizioni generali e al quadro complessivo della malattia vescicale oltre alle possibili implicazioni per la Sua qualità di vita successiva all’intervento.
Di seguito Le presentiamo le differenti possibilità di derivazioni urinarie realizzabili con tecnica robotica presso il nostro centro:
- NEOVESCICA ILEALE ORTOTOPICA
- URETEROILEOCUTANEOSTOMIA (BRICKER)
- URETEROCUTANEOSTOMIA (UCS)
1) NEOVESCICA ILEALE ORTOTOPICA
Nel caso in cui il paziente sia in buone condizioni generali e la malattia, durante l’intervento chirurgico, risulti confinata alla vescica senza coinvolgimento dell’uretra e degli ureteri, la derivazione urinaria che si prospetta più frequentemente è una neovescica ortotopica, cioè la ricostruzione di una vescica nuova utilizzando un segmento di circa 40-60 cm di intestino ileale, adeguatamente configurato in modo da assumere l’aspetto di una cavità sferoidale a cui vengono abboccati gli ureteri. Dopo aver prelevato il segmento intestinale necessario per creare la nuova vescica verrà ripristinata la continuità dell’intestino tramite l’utilizzo di suturatrici meccaniche. Esistono diversi tipi di conformazioni neovescicali, la scelta dipenderà dalla conformazione del paziente e dal chirurgo. La neovescica viene posizionata nello scavo pelvico e anastomizzata, ossia “ri-agganciata”, al tratto rimanente dell’uretra. La neovescica funzionerà come serbatoio per l’urina, e dovrà essere svuotata periodicamente.
Il paziente dovrà inoltre essere motivato e consapevole della necessità di una riabilitazione per apprendere il nuovo modo di urinare. Infatti lo stimolo minzionale verrà avvertito come sensazione di ripienezza o vago dolore sovrapubico. La minzione si attuerà attraverso la compressione della neovescica dopo aver rilasciato la muscolatura del piano perineale ed avverrà aumentando la pressione dei muscoli addominali o con la compressione manuale. Potrebbe essere necessario nei primi mesi dopo l’intervento svuotare questo nuovo serbatoio eseguendo dei cateterismi cioè inserendo periodicamente nell’arco della giornata un piccolo catetere che svuoti la vescica. Il nostro personale medico ed infermieristico sarà lieto di insegnarLe questa manovra che risulta sia di facile apprendimento che di esecuzione. Altra possibile situazione potrebbe essere una parziale incontinenza urinaria, particolarmente durante le ore notturne.
Inoltre i pazienti dovranno assumere alcune compresse di bicarbonato per ridurre l’acidosi metabolica che si sviluppa in seguito al riassorbimento ad opera del segmento intestinale utilizzato per la configurazione della neovescica.
2) URETEROILEOCUTANEOSTOMIA (BRICKER)
Il confezionamento della neovescica è controindicato in alcuni casi:
• Malattia non confinata alla vescica
• Coinvolgimento neoplastico dell’uretra
• Coinvolgimento neoplastico degli ureteri
• Stato di decadimento generale del paziente
• Necessità di assistenza da parte del paziente
• Incontinenza urinaria preoperatoria
• Pregressa radioterapia
• Funzionalità renale di partenza non ottimale
• Patologie intestinali (Retto colite ulcerosa, Morbo di
Chron, patologie da malassorbimento, pregresse neoplasie intestinali, pregressi interventi chirurgici intestinali)
• Conformazione del paziente, per cui potrebbero venire meno i vantaggi della neovescica.
In questi casi si opterà per un altro tipo di derivazione urinaria chiamata uretero-ileo-cutaneostomia. In questo caso si utilizza un segmento di 15-20 cm di intestino (ileo), a cui vengono abboccati gli ureteri. L’uretere di sinistra viene mobilizzato e controlateralizzato a destra per poter essere connesso al tratto intestinale isolato. Dopo avere ripristinato la continuità intestinale il segmento prelevato verrà anastomizzato, ossia “attaccato”, alla cute a livello del quadrante inferiore destro dell’addome.
È sicuramente la tecnica più utilizzata. L’urina, che defluisce continuamente attraverso gli ureteri e il condotto ileale, viene raccolta in un sacchetto applicato con adesivo in corrispondenza della stomia cutanea.
Il sacchetto è provvisto di una via di uscita per mezzo della quale può essere svuotato periodicamente. La cura del sacchetto di raccolta delle urine è facile e il paziente viene adeguatamente istruito a questo proposito. Il sacchetto andrà cambiato periodicamente.
La presenza della stomia, per quanto in genere difficile all’inizio da accettare, non compromette irrimediabilmente la qualità di vita del paziente se istruito all’utilizzo corretto e a piccoli espedienti atti a rendere la vita quotidiana la più normale possibile. Anche con questa derivazione i pazienti potrebbero dover assumere alcune compresse di bicarbonato per ridurre l’acidosi metabolica che si sviluppa in questi casi.
3) URETEROCUTANEOSTOMIA (UCS) MONO O BILATERALE
Consiste nel mettere in comunicazione gli ureteri direttamente all’esterno sulla cute, per permettere all’urina di defluire all’esterno, e raccoglierla in due sacchetti (UCS bilaterale), o in un sacchetto (UCS monolaterale), analoghi a quelli già descritti per la ureteroileocutaneostomia, che dovranno essere sostituiti a giorni alterni. L’UCS può essere una soluzione definitiva, per permettere una radioterapia o in casi in cui non sia utilizzabile l’intestino. Viene inoltre posizionato un catetere all’interno dell’uretere, per evitare il restringimento della stomia, che verrà sostituito periodicamente ogni 3-6 mesi.
Nel corso dell’intervento vengono posizionati:
• Un sondino nasogastrico, che viene di solito al termine dell’intervento oppure la giornata successiva
• Un drenaggio nello scavo pelvico, normalmente rimosso tra la quarta e la decima giornata;
• Due tutori ureterali, che vendono di solito rimossi in decima-dodicesima giornata con una variabilità legata alla tecnica chirurgica eseguita.
• Incasodineovescicaortotopica,vieneposizionatoanche un catetere neovescicale cche fuoriesce dal meato uretrale
Il paziente viene fatto alzare dal letto già in prima giornata post operatoria e, compatibilmente con la naturale ripresa delle sue energie, viene mobilizzato in misura sempre maggiore. È bene che il paziente, non appena possibile, inizi a passeggiare nel corridoio per favorire la ripresa della normale circolazione, per evitare la formazione di trombi nelle vene degli arti inferiori e per facilitare la ripresa della attività intestinale.
Nel frattempo viene mantenuto la terapia antidolorifica che viene progressivamente ridotta da continua a “al bisogno”: questo passaggio viene effettuato gradualmente al fine di garantire il controllo del dolore favorendo tuttavia la ripresa del funzionamento intestinale che viene rallentata dai farmaci analgesici.
Nel post operatorio, compatibilmente con il rischio di sanguinamento, verrà impostata una profilassi della patologia tromboembolica con eparina a basso peso molecolare, che verrà proseguita per 20-30 giorni. Al paziente verrà insegnato come eseguire la somministrazione del farmaco sottocute. Inoltre verranno fornite precise indicazioni sulla ripresa di eventuali terapie domiciliari.
Il paziente potrà iniziare a bere ed alimentarsi in modo graduale già dalla giornata successiva all’intervento, compatibilmente con la ripresa della motilità intestinale. Le verrà proposto di masticare chewing-gum alla frutta (tipo “bubble-gum”) già alcune ore dopo la fine dell’intervento e di succhiare caramelle alla frutta tipo “gelèe”: ciò stimola la ripresa nella naturale peristalsi intestinale. Poi verranno progressivamente introdotti omogeneizzati alla frutta, alla carne, yogurt, gelati e quinti cibi solidi. La ripresa dell’alimentazione dovrà avvenire progressivamente e con prudenza e se il paziente lo gradisce. La ripresa dell’alimentazione è comunque auspicabile, per contrastare tutti gli effetti negativi dello stress chirurgico e per riprendere quanto prima il suo equilibrio, procedendo verso la guarigione.
Si prevede una degenza che varia tra 8 ed i 15 giorni in funzione della derivazione urinaria utilizzata, salvo complicazioni. La preghiamo di tenere presente che il confezionamento di una neovescica ha tempi di degenza spesso più lunghi rispetto alle altre derivazioni.
Che cos’è la nefrectomia parziale? L’intervento prevede l’asportazione
di cellule tumorali del rene (o neoplasia) e garantisce il mantenimento di un margine di sicurezza di tessuto sano e la preservazione del restante parenchima renale.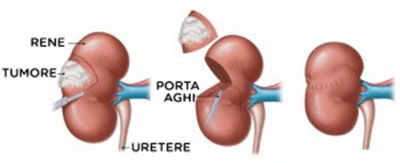
Secondo le linee guida internazionali, in caso di tumore al rene, la filosofia strategica è quella di proporre una chirurgia conservativa (nephron sparing) in tutti i casi in cui questo, considerate dimensioni, sede ed eventuali compressioni, sia tecnicamente ed oncologicamente possibile. Questo consente di preservare al massimo la funzionalità residua dell’organo.
Fino all’inizio degli anni ’90, la nefrectomia parziale si eseguiva esclusivamente “a cielo aperto”, ossia praticando un accesso lombotomico o addominale, vi erano alcune remore relativamente alle possibili problematiche di efficacia oncologica della laparoscopia, motivo per cui la chirurgia laparoscopica oncologica renale era confinata presso alcuni centri pionieristici di elezione, dedicati alla laparoscopia urologica.
Negli anni, l’evidenza di una adeguatezza oncologica della laparoscopia nel trattamento dei tumori renali, con risultati equivalenti alla tecnica a cielo aperto, associata alla corretta codifica delle tecniche chirurgiche mininvasive da un lato e dallo sviluppo tecnologico dall’altro ha consentito un’accettazione sempre più ampia da parte della comunità urologica di questo intervento, con conseguente progressiva e capillare diffusione.
Oggi a questa pratica si è aggiunta la nefrectomia parziale robotica che rappresenta l’evoluzione della tecnica laparoscopica. Questa tecnica si avvale dell’ausilio del sistema robotico e consente l’esecuzione di un intervento conservativo minimamente invasivo anche in casi particolarmente complessi.
La nefrectomia parziale viene eseguita in anestesia generale. Il paziente viene posizionato sul fianco.
L’intervento ha una durata che va dai 90 ai 180 minuti; vengono praticate 4/5 incisioni addominali (0.5 – 1 centimetri circa), delle quali una viene ampliata, al termine dell’intervento, per l’estrazione del pezzo operatorio. Si può inoltre prevedere un’incisione aggiuntiva per il sollevamento del fegato.
L’intervento di nefrectomia parziale può essere eseguito per via transperitoneale (più comune) o per via retroperitoneale.
Nel caso di nefrectomia parziale per via transperitoneale, dopo aver inciso la doccia parietocolica si accede al rene, liberandolo dal grasso circostante allla loggia renale. Una volta che il tumore è stato identificato, si procede con l’isolamento dei vasi.
Al fine di garantire una resezione ottimale della neoplasia, la nefrectomia parziale include spesso l’interruzione temporanea del flusso sanguigno al rene (ischemia calda). Alla fine della resezione, si esegue quindi una doppia sutura sul letto di resezione, permettendo così la chiusura dei vasi arteriosi e venosi e la ricostruzione della capsula renale.
La nefrectomia parziale si conclude con il posizionamento di un tubo di drenaggio (che verrà rimosso generalmente dopo 2-3 giorni dall’intervento). I tempi di degenza sono normalmente compresi fra 3 e 5 giorni.
L’intervento di asportazione radicale della prostata viene generalmente eseguito da 4 a 8 settimane dopo l’esecuzione delle biopsie prostatiche e, generalmente, non meno di 12 settimane dopo essere stati sottoposti ad eventuale intervento di resezione/enucleazione endoscopica di adenoma prostatico.Vengono mantenuti questi intervalli di tempo in modo tale che possano risolversi eventuali aderenze infiammatorie e/o ematomi in sede prostatica, permettendo così all’anatomia della ghiandola di ritornare normale.Questo è particolarmente importante per i pazienti candidati alla preservazione dei fasci neuro-vascolari implicati nel controllo dell’erezione peniena e della continenza urinaria.
L’intervento di prostatectomia radicale robotica viene eseguito in anestesia generale, dopo somministrazione in reparto, prima di essere portato nella sala operatoria, dei farmaci della preanestesia, che permettono al paziente di giungere in sala operatoria più sereno e tranquillo.
Contemporaneamente all’inizio delle manovre anestesiologiche viene iniziata la somministrazione endovenosa di farmaci per la terapia del dolore (analgesia preventiva) che viene opportunamente prolungata nel post operatorio per 24 ore. Il controllo del dolore in tal modo è ottimale e il paziente supera velocemente il trauma dell’intervento, peraltro minimizzato dall’assenza di incisioni muscolari.
La minima invasività di questa particolare tecnica chirurgica fa si’ che il paziente sia di solito in grado di iniziare a bere, alimentarsi e mobilizzarsi già a partire dalla serata successiva all’intervento.
La prevenzione dei fenomeni trombotici e trombo-embolici viene attuata dal posizionamento, prima dell’inizio dell’intervento, di calze elastiche agli arti inferiori, dalla somministrazione di un farmaco anticoagulante sottocute a partire dalla sera successiva all’intervento e dalla precoce mobilizzazione del paziente stesso. Una volta tornato nel Suo letto di reparto, potrà muoversi, girarsi su un fianco o sull’altro, mettersi semiseduto; non dovrà cioè stare immobile.
Tutte le procedure descritte sono volte a garantire al paziente la rapida ripresa del benessere fisico e psichico e a minimizzare le conseguenze dello stress operatorio.
Il primo tempo dell’intervento consiste nella creazione del pneumoperitoneo: la cavità addominale deve essere riempita di anidride carbonica per creare una camera di lavoro per gli strumenti chirurgici robotici.
Una incisione di circa 2 cm a livello sopra-ombelicale consente di posizionare sotto visione diretta e in maniera del tutto atraumatica il primo trocar robotico attraverso il quale si inserisce l’ottica che permetterà al chirurgo di eseguire l’intervento.
Si inseriscono successivamente in cavità peritoneale altri 5 trocar operativi, di cui tipicamente 3 gestiti dal primo operatore e 2 dall’assistente.
La premessa da considerare prima di descrivere l’intervento nei dettagli è che la tecnica robotica consente di operare con un ingrandimento visivo fino a circa 20 volte e con una visione a 3 dimensioni. Questo permette al chirurgo di apprezzare la profondità di campo, cosa non possibile ad esempio con la tecnica laparoscopica classica. La visione intraoperatoria robotica permette di riconoscere anche i più piccoli dettagli anatomici e di eseguire l’intervento con una accuratezza significativamente superiore a quanto sia possibile ottenere con la chirurgia classica a cielo aperto o con la chirurgia laparoscopica classica.
Il primo tempo operatorio è rappresentato dall’isolamento delle vescicole seminali attraverso una piccola breccia eseguita nel peritoneo parietale che riveste il cavo del Douglas, al di sopra dell’intestino retto. Questo approccio permette una perfetta visualizzazione delle vescicole seminali e, in particolare, sia dei vasi sanguigni che dei nervi che le avvolgono. Queste ultime strutture vengono conservate e si ha cura di non usare mai energia termica per non danneggiare il ricco plesso nervoso peri-vescicolare dove transitano rami nervosi diretti ai corpi cavernosi del pene e responsabili dell’erezione peniena.
Completato l’isolamento delle vescicole seminali, dalla cavità peritoneale si accede allo spazio pelvico dove è localizzata la prostata.
Nel caso in cui fosse oncologicamente necessario – cioè quando i parametri pre-operatori lo consigliassero – si procede alla rimozione dei linfonodi pelvici (linfoadenectomia), a cui afferisce la linfa prodotta dalla prostata, bilateralmente. I linfonodi sono piccoli organelli che hanno la funzione di filtrare liquidi e proteine provenienti da tutto l’organismo. Quando un organo si ammala di tumore è possibile che alcune cellule tumorali escano dai confini dello stesso e vengano catturate dai linfonodi più vicini. Per questo motivo in alcuni pazienti con tumore della prostata la rimozione dei linfonodi viene eseguita al fine di ottenere una più precisa stadiazione della malattia e anche perché la rimozione di eventuali linfonodi ammalati può avere un effetto curativo. La tecnica robotica permette di eseguire, quando necessario, linfoadenectomie estremamente estese ed accurate e quindi si presta a essere utilizzata con successo anche in pazienti con tumore della prostata avanzato.
La rimozione della prostata avviene per via anterograda, partendo cioè dal collo vescicale che viene separato dalla base della prostata avendo cura di conservare il più possibile l’integrità delle fibre muscolari del collo vescicale stesso le quali compartecipano al meccanismo della continenza urinaria.
Completata questa manovra, si raggiungono le vescicole seminali precedentemente isolate e si identifica il piano di scollamento prostatico partendo alle ore 6.
A seconda delle caratteristiche della malattia (malattia palpabile o meno alla esplorazione rettale, percentuale delle biopsie positive per tumore, aggressività del tumore rilevato nelle biopsie – Gleason score, PSA preoperatorio, risultati della risonanza magnetica) si identifica un piano intrafasciale (estremamente aderente alla capsula prostatica) o interfasciale (lievemente più distante dalla capsula prostatica ma sempre ponendo la massima attenzione per salvaguardare i nervi che avvolgono la prostata) e si procede nell’isolamento anterogrado della prostata.
L’isolamento della prostata viene eseguito ponendo massima attenzione nell’evitare l’uso di qualsiasi energia termica al fine di evitare danni al tessuto nervoso periprostatico. L’emostasi viene ottenuta con l’applicazione di microclip (2 mm) in titanio o con piccolissimi punti di sutura.
In alcuni pazienti nei quali il tumore prostatico dimostri pre- o intraoperatoriamente di coinvolgere anche la ricca ragnatela di nervi che avvolge la ghiandola prostatica, di necessità questa deve essere sacrificata in parte o totalmente per permettere la rimozione radicale del tumore e ridurre il rischio di margini positivi all’esame istologico. In questi casi la ripresa dell’erezione peniena può essere molto rallentata o può crearsi un danno permanente all’erezione.
La sezione del plesso venoso di Santorini e la sua successiva sutura emostatica con punti posti sotto visione diretta viene effettuata ponendo la massima attenzione alla preservazione della integrità dello sfintere uretrale esterno, muscolo principale responsabile della continenza urinaria.
Si seziona quindi l’uretra a livello dell’apice prostatico e a questo punto il pezzo operatorio prostatico, completamente liberato, viene estratto dall’addome attraverso una porta operativa. Quando necessario, viene eseguito un esame istologico intraoperatorio al congelatore per valutare la integrità dei margini chirurgici prostatici.
L’intervento procede con la accurata cura dell’emostasi: ogni eventuale piccola fonte di sanguinamento viene controllata sempre e per quanto possibile con mini clip e mini punti di sutura.
L’anastomosi uretro-vescicale viene eseguita con una sutura in continua che garantisce una tenuta eccellente e rapida ripresa della continenza urinaria. Si posiziona un catetere vescicale e viene eseguita prova di tenuta dell’anastomosi stessa.
Si posiziona nello scavo pelvico un piccolo tubo di drenaggio che permette il monitoraggio di eventuali perdite di sangue, di urine o di linfa.
La tecnica prevede la possibilità di preservare da un solo lato oppure bilateralmente i fasci neuro-vascolari che sono coinvolti nel meccanismo dell’erezione. La possibilità di preservarli dipende dalla situazione anatomica locale del paziente, dalla situazione oncologica, cioè dalla eventuale estensione della malattia della prostata, e da fattori anatomo-chirurgici, cioè dalla possibilità tecnica di realizzare un tale tipo di intervento.
Già a 18 ore dalla fine dell’intervento il paziente può solitamente riprendere a bere e ad alimentarsi in modo progressivo. Il paziente viene fatto alzare da letto già in serata o in prima giornata postoperatoria e, compatibilmente con la naturale ripresa delle sue energie, viene mobilizzato in misura sempre maggiore. È bene che il paziente, non appena si senta in grado, faccia passeggiate nel corridoio, favorendo la ripresa della normale circolazione, per evitare la formazione di trombi alle vene degli arti inferiori e per facilitare la ripresa della attività intestinale.
Il catetere vescicale, che viene posizionato durante l’intervento, viene mantenuto in sede per un periodo di solito variabile da 5 a 10 giorni, a seconda delle condizioni locali intra-operatorie e del decorso post-operatorio. In rare occasioni può essere necessario mantenere il catetere vescicale in sede più a lungo, ma generalmente non oltre 3 settimane.
Il paziente che viene dimesso dall’ospedale con catetere vescicale a dimora riceve un appuntamento per ritornare dopo alcuni giorni nei nostri ambulatori per rimuoverli.
L’esame istologico definitivo della prostata e dei linfonodi eventualmente rimossi nel corso dell’intervento diviene usualmente disponibile in circa 15 giorni. L’esame istologico definitivo chiarisce l’estensione e la aggressività del tumore prostatico. In particolare i parametri che vengono considerati sono: 1. Sede del tumore e sua relazione con i margini di resezione chirurgica; 2. Aggressività del tumore; 3. Volume del tumore; 4. Diffusione del tumore: contenuto all’interno della prostata oppure con diffusione all’esterno della prostata; 5. Infiltrazione da parte del tumore delle vescicole seminali oppure dei linfonodi rimossi (ricordo che non tutti i pazienti operati necessitano della rimozione dei linfonodi).
L’esame istologico definitivo rappresenta quindi un elemento essenziale per decidere se il paziente deve eseguire cure addizionali o meno. È peraltro vero che, sempre più di frequente, anche di fronte a parametri prognostici potenzialmente sfavorevoli come ad esempio: alta aggressività della malattia, margini chirurgici positivi, estensione extra capsulare della malattia, infiltrazione delle vescicole seminali, metastasi linfonodali, si tende a verificare il primo dosaggio del PSA eseguito tipicamente 3 mesi dopo l’intervento poiché, se questo fosse completamente azzerato, il paziente potrebbe essere solamente osservato con attenzione nel tempo.
Se si considerano tutti i pazienti operati, indipendentemente dall’operatore, la ripresa completa della continenza urinaria senza necessità di utilizzare pannolini si è osservata a 3, 6 e 12 mesi dopo l’intervento in circa il 60%, 80% e 95% dei pazienti. Queste percentuali dipendono in modo significativo da tre fattori: 1. Chirurgo che esegue l’intervento; 2. Età del paziente e condizioni fisiche generali (in particolare presenza o meno di disturbi urinari prima dell’intervento e livello di sovrappeso corporeo); 3. Stadio di malattia prostatica.
La ripresa completa della erezione peniena nei pazienti con funzione sessuale perfetta prima dell’intervento si è osservata a 3, 6 e 12 mesi dopo l’intervento in circa il 30%, 50% e 70% dei pazienti. Queste percentuali dipendono in modo significativo da tre fattori: 1. Chirurgo che esegue l’intervento; 2. Età del paziente; 3. Eventuali fattori di rischio per disfunzione erettile presenti prima dell’intervento (ad es. pressione alta, obesità, diabete mellito, fumo di sigaretta).
Nella nostra esperienza la ripresa della continenza urinaria e della erezione peniena sono risultate significativamente migliori nei pazienti operati con tecnica robotica rispetto a coloro che sono stati operati con tecnica classica a cielo aperto.
